Nyfødtveileder
9 Nevrologi, sanser og mishandling
9.13 Hørselsundersøkelser/hørselsscreening
Sist faglig oppdatert: 22.03.2026
Dagny Hemmingsen, Claus Klingenberg, Ragnhild Støen og Tone S. Mattson
Bakgrunn
- Medfødt moderat og alvorlig hørseltap har en prevalens på rundt 1–3 per 1000 fødsler.
- Omtrent halvparten av barn med medfødt hørseltap har ingen kjente risikofaktorer.
- Hørselsscreening i nyfødtperioden gjør at man kan finne pasientene tidligere og derved raskt komme i gang med habiliteringstiltak som har stor prognostisk betydning.
Målet er at små barn med hørselstap skal være diagnostisert innen 3 måneders alder, at høreapparat skal være tilpasset innen 6 måneders alder, og at barn med de mest alvorlige hørselstapene skal få cochlea implantat (CI) innen 12 måneders alder.
Det finnes to metoder for Hørselsscreening i nyfødtperioden:
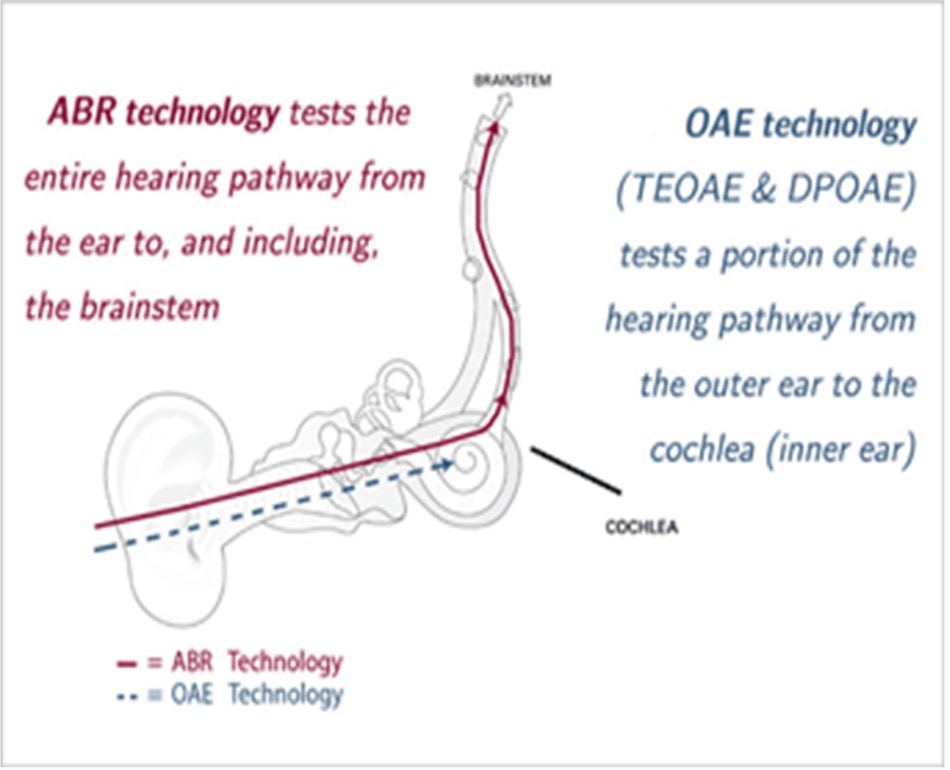
- Otoakustiske emisjoner (OAE): Påviser både konduktive hørseltap og kokleær dysfunksjon, noe som er anslått å utgjøre rundt 99 % av tilfellene av medfødt hørselstap hos barn som ellers ser friske ut ved fødsel. OAE kan være vanskelig å gjennomføre første levedøgn (0–24 timer) pga. rester av sekret, fostervann etc. i øregangen. OAE er ellers teknisk enklere enn AABR, men har noe høyere andel falsk positive.
- Automatisert hjernestammeaudiometri (AABR): Påviser også hørseltap på et retrokokleært nivå (hørselsnerve og hjernestamme). Retrokokleære hørselstap hos nyfødte kan være forårsaket av auditiv nevropati eller cerebrale skader, noe man ser hyppigere hos syke nyfødte innlagt nyfødt intensiv avdeling. AABR er noe mer tidkrevende og teknisk utfordrende enn OAE, da det kreves både elektroder på panne, nakke og kinnben, i tillegg til øreplugg. AABR er ikke validert for barn < 34 uker.
Gjennomføring av nyfødtscreening av hørsel og oppfølging
Sosial- og Helsedirektoratet anbefalte i 2008 hørselscreening av alle nyfødte barn. I 2016 publiserte Helsedirektoratet reviderte faglige retningslinjer for hørselsscreening i nyfødtperioden: https://helsedirektoratet.no/retningslinjer/screening-av-horsel-hos-nyfodte.
- Alle nyfødte barn skal tilbys hørselsscreening i regi av barsel- eller nyfødtavdeling.
- Friske nyfødte uten risikofaktorer for auditiv neuropati skal screenes med OAE.
- Syke nyfødte med utvalgte risikokriterier for auditiv neuropati (se under) skal screenes med AABR.
- Barn som ikke passerer screening med OAE (test og retest) skal også undersøkes med AABR.
Det nyfødtmedisinske fagmiljøet har, i samråd med det barneaudiologiske fagmiljøet, valgt følgende definisjon av barn som bør screenes med AABR.
- Premature < 32 uker/FV < 1500 g
- Hypotermibehandling pga. alvorlig fødselsasfyksi
- Minst én bilirubinverdi i blod > 500 mikromol/L
- Gjennomgått alvorlig hjerneblødning (IVH grad III–IV eller annen parenkymatøs hjerneblødning), cystisk PVL, hjerneinfarkt/slag.
- Cerebrale misdannelser
- Ototoksiske medikamenter (furosemid, aminoglykosider, glykopeptidantibiotika) brukt samtidig med alvorlig nyresvikt
- Medfødt infeksjon med CMV eller toxoplasmose
- Gjennomgått CNS infeksjon (meningitt/encefalitt)
Gjennomføring av OAE og AABR
Barnet må undersøkes i omgivelser uten støy, og barnet bør være rolig (nymatet).
Øresonden settes inn mens man forsiktig drar i øret for å "rette ut" øregangen.
OAE:
Resultatet på testen er enten "pass" (godkjent) eller "refer" (ikke godkjent).
- Ved "pass" på begge ører anses hørselen som normal (negativt funn).
- Ved "refer" på ett eller begge ører bør OAE gjentas minimum to ganger; første gang samme dag og hvis fortsatt «refer» gjenta neste dag.
- Dersom OAE ikke passeres etter disse to trinnene, eller barnet fyller minst et av risikokriteriene over, gjøres AABR.
AABR utføres fortrinnsvis på barsel eller nyfødt intensiv dersom utstyret er tilgjengelig; alternativt må det henvises til Høresentral for AABR.
Oppfølging etter screening
- Resultatet av OAE og AABR dokumenteres i barnets elektroniske journal.
- Ved ikke passert nyfødtscreening (OAE og/eller AABR) henvises barnet til høresentral.
- Ved ikke passert nyfødtscreening på ett eller begge ører skal det tas CMV prøve i spytt. Se eget avsnitt under. Det må utarbeides lokale prosedyrer for videre henvisning til høresentralen av barn som ikke passerer hørselsscreeningen, eller som av andre grunner skal følges på høresentralen.
CMV testing av nyfødte som ikke passerer hørselsscreening
Barn med medfødt CMV infeksjon har økt risiko for hørselstap, både medfødt og med debut senere i barnealder. Utvidet oppfølging i denne gruppen er derfor anbefalt.
- Nyfødte som ikke passerer hørselscreeningen, bør ta spyttprøve for å identifisere en mulig medfødt CMV-infeksjon.
- Positiv CMV-PCR i spytt skal alltid bekreftes med CMV-PCR i urin. Ved en medfødt CMV infeksjon er det nesten alltid svært høy virusutskillelse i urin, og CMV-PCR i urin er meget sjelden falsk positiv.
- Det anbefales at alle avdelinger har gode rutiner for prøvetaking (spyttprøve) hvis ikke barnet har bestått hørselsscreening eller ikke kan hørselsscreenes innen 2–3 uker etter fødsel (f.eks. premature).
- Positiv spyttprøve kontrolleres med urinprøve før barnet er 14–21 dager for å kunne skille mellom medfødt CMV og postnatal transmisjon eller smitte..
- NB. Ved positiv spyttprøve informeres foreldrene om at den kan være falsk positiv og at man derfor må kontrollere med urinprøve som er mer presis.
- Se ellers eget avsnitt om CMV infeksjoner for videre oppfølging hvis spyttprøven er positiv og om ev. antiviral behandling hvis en medfødt CMV infeksjon.
Barn med risiko for hørselstap som kan oppstå etter passert screening i nyfødtperioden - anbefalinger om oppfølging i høresentral
Anbefaling er basert på en litteraturgjennomgang i 2025 og vurdert i sammenheng med eksisterende oppfølgingsprogrammer for syke nyfødte og helsestasjonens oppfølging av hørsel.
Følgende barn bør henvises til høresentral ved utskrivelse fra barsel/nyfødt intensiv for videre oppfølging, uavhengig av resultat på hørselsscreening i nyfødtperioden:
- Medfødt infeksjon med CMV eller toksoplasmose
- Gjennomgått behandling på ECMO eller åpen hjertekirurgi (hjerte-lungemaskin)
- Hypotermibehandling pga. alvorlig fødselsasfyksi
- Syndromer assosiert med hørselstap og kraniofaciale misdannelser (inkl. barn med leppe- kjeve-ganespalte)
- Hørselstap hos førstegradsslektning (foreldre eller søsken)
- Bakteriell meningitt og/eller meningokokksepsis*
For alle disse barna, utenom de med meningitt (se under), anbefales det henvisning til Høresentral for oppfølging ved 9–12 md. alder.
*Disse skal raskt henvises til høresentral og få time innen 4–6 uker etter påvist infeksjon. Meningitt kan forårsake alvorlige hørselstap med kalsifisering i cochlea, som kan hindre cochleaimplantasjon. For å bevare hørselen må operasjonen utføres før kalsifisering oppstår, og rask utredning er derfor avgjørende.
Referanser
- Yoshinaga-Itano C, et al. Language of early-and later-identified children with hearing loss. Pediatrics. 1998; 102:1161-71
- Gantt S, et al. Cost-effectiveness of Universal and Targeted Newborn Screening for Congenital Cytomegalovirus Infection. JAMA Pediatr. 2016; 170:1173-80.
- Williams EJ, et al. First estimates of the potential cost and cost saving of protecting childhood hearing from damage caused by congenital CMV infection. Arch Dis Child Fetal Neonatal Ed. 2015; 100:F501-6.
- Kimberlin D. Valganciclovir for Symptomatic Congenital CMV Disease. NEJM 2015; 372:933-43.
- Leruez-Ville M, et al. Consensus recommendation for prenatal, neonatal and postnatal management of congenital cytomegalovirus infection from the European congenital infection initiative (ECCI). Lancet Reg Health Eur 2024; 40:100892.
- Hemmingsen D, et al. Sensorineural hearing impairment among preterm children- a Norwegian population-based study. Arch Dis Child Fetal Neonatal Ed. 2024; 110:68-74.
- Hemmingsen D, et al. Hearing impairment after asphyxia and neonatal encephalopathy: a Norwegian population-based study. Eur J Pediatr 2024; 183:1163-72.
- Kettler M, et al. American Academy of Audiology Position Statement on Early Identification of Cytomegalovirus in Newborns. J Am Acad Audiol. 2023; 34(3-04):84-9.
- Rohren L, et al. Congenital Cytomegalovirus-Associated Sensorineural Hearing Loss in Children: Identification Following Universal Newborn Hearing Screening, Effect of Antiviral Treatment, and Long-Term Hearing Outcomes. Ear Hear. 2024. 45:198-206.
- Olds C, et al. Bilirubin-Induced Audiologic Injury in Preterm Infants. Clin. Perinatol. 2016; 43:313-23.
- American Academy of Pediatrics Joint Committee on Infant Hearing. Year 2019 Position Statement: Principles and Guidelines for Early Hearing Detection and Intervention Programs. J Early Hear Detect Interv. 2019; 4:1-44.
- Fitzgibbons, et al. Childhood hearing loss detected beyond the newborn screen. International Journal of Audiology 2023; 62:278-85.
- Mackey AR, et al. Pre-school hearing screening is necessary to detect childhood hearing loss after the newborn period: a study exploring risk factors, additional disabilities, and referral pathways. International Journal of Audiology 2025; 64:80-8.
- Rodenburg-Vlot MBA, et al. Systematic Review: Incidence and Course of Hearing Loss Caused by Bacterial Meningitis: In Search of an Optimal Timed Audiological Follow-up. Otol Neurotol. 2016 37:1-8.
- Dodds A, et al. Cochlear implantation after bacterial meningitis: the dangers of delay. Arch Dis Child 1997; 76:139-40.
Tidligere versjoner:
2021 og 2023 Claus Klingenberg og Mona Mørkved
Ved tilbakemeldinger eller spørsmål, send en mail til veiledere@barnelegeforeningen.no.










